LISTA DE EXERCÍCIOS PARA AR2/2
LISTA DE EXERCÍCIOS DE REVISÃO – AR2
1. As células são as unidades funcionais e estruturais dos seres vivos. Apesar da variedade dos tipos celulares, algumas partes são encontradas em todas as células. Costuma-se dizer que essa estrutura é formada por membrana plasmática, citoplasma e núcleo, uma informação incorreta. Explique essa afirmação detalhadamente usando os postulados da teoria celular e os modernos conhecimentos sobre as células.
Logo, a Teoria celular pode ser dividida em três postulados:
1) Todos os organismos vivos são compostos de uma ou mais células;
2) A célula é a unidade básica de estrutura e organização nos organismos;
3) As células surgem de células pré-existentes.
De acordo com a teoria todos os seres vivos são formados por células, entretanto existem organismos, como os vírus, que não são formados por células, e existem organismos que não possuem núcleo, mas um nucleóide.
Todos os organismos são formados por células mas nem todas as células possuem núcleo, por exemplo as bactérias que possuem nucleóide ao invés de núcleo.
2. Desenhe uma célula animal e uma célula vegetal, coloque as seguintes organelas RER, REL, mitocôndria, cloroplasto, lisossomo, vacúolo, nucléolo, complexo golgiense, ribossomo, localize a membrana celular em ambas e a parede celular.
As células eucariontes possuem um envoltório nuclear, e as procariontes possuem material genético, fixo no mesossomo, em contato direto com o citoplasma. Dos organismos citados a seguir, qual apresenta células procariontes? Justifique sua
resposta.
(A) Mamíferos.
(B) Lactobacilos.
(C) Fungos.
(D) Levedura.
(E) Protozoários.
Justificativa
Os lactobacilus são bactéreias benéficas ao organismo são denominados de procariotos por não apresentarem carioteca. O material genético dessas células fica concentrado em uma região que é denominada nucleoide (uma invaginação da membrana plasmática). Essas células também não apresentam organelas membranosas e sua respiração celular se dá toda através da membrana plasmática.
4. Coloque o nome nas estruturas do sistema digestório e dê sua função.
1. Glândulas salivares: umedecem os alimentos com saliva que é proteina (a saliva é composta por proteínas salivares, como mucinas, cistatinas, imunoglobulina A (IgA ), amilase e estaterina. De todas essas proteínas a mais importantes para a digestão é a amilases salivar que atua sobre carboidratos.
2. Esôfago, é responsável por levar a comida ingerida até o estômago.
3. Estômago: é um órgão do sistema digestório que armazena alimento e dá início à digestão das proteínas. É no estômago que o suco gástrico é produzido. O estômago secreta enzimas e hormônios. O estômago é o órgão do sistema digestório onde tem início o processo de digestão de proteínas.
4. Fígado: a função mais conhecida do fígado seja a de filtragem do sangue e eliminação de toxinas. Isso inclui substâncias que são absorvidas pelo intestino e medicamentos, por exemplo. Para que essas toxinas sejam eliminadas, o sangue passa por uma filtragem no fígado.
O fígado é o segundo maior órgão, perdendo apenas para a pele, e a maior glândula do corpo humano. Ele apresenta várias funções essenciais para o funcionamento do organismo, como a eliminação de substâncias tóxicas e a produção da bile, um produto essencial para a digestão de gorduras. Uma das doenças que acometem o fígado é a cirrose, a qual pode ser causada pelo alcoolismo e por doenças, como as hepatites B e C.
5. Vesícula Biliar: órgão em forma de saco, parecida com uma pera, localizada abaixo do lobo direito do fígado. Sua função é armazenar a bile, líquido produzido pelo fígado que atua na digestão de gorduras no intestino.
6. Intestino delgado: é o órgão responsável pela absorção dos alimentos, permitindo que os minerais, as vitaminas e nutrientes sejam aproveitados pelo organismo.
A. Local por onde passa alimento e o ar que respiramos ( I )
B. Local onde começa a digestão de proteínas. Produz o suco gástrico. ( III )
C. Produz o suco pancreático com uma mistura de enzimas para cada grupo de macronutrientes ( IV )
D. Local onde ocorre a maior absorção de água e formação do bolo fecal. ( V )
E. Responsável para produção de bile para dissolver gorduras. ( X )
F. Tubo muscular que leva o bolo alimentar da boca ao estômago através de movimentos peristálticos ( II )
G. Local onde ocorre a maior absorção dos nutrientes. ( VI )
O chamado suco pancreático, produzido pelo pâncreas, atua no processo de digestão. Essa solução é rica em bicarbonato, o qual atua neutralizando o material vindo do estômago (quimo). Além de bicarbonato, são encontradas enzimas, as quais são ativadas apenas quando chegam ao duodeno (parte do intestino delgado). São enzimas encontradas no suco pancreático as amilases pancreáticas (agem nos carboidratos), tripsina e quimiotripsina pancreáticas (agem nas proteínas), lipase pancreática (age nas gorduras) e nucleases pancreáticas (agem nas gorduras).
6. O esqueleto humano pode ser dividido em axial e apendicular. Entre os ossos citados abaixo, marque o único encontrado no esqueleto apendicular.
( A ) Crânio
( B ) Esterno
( C ) Costelas
( D ) Vértebras
( E ) Úmero
Luxação do ombro (úmero)
A luxação se refere à perda da congruência articular entre dois ossos. Em outras palavras, a articulação perde sua anatomia habitual porque um dos ossos se desarticula do outro movendo-se em outra direção. Os termos populares mais comuns para esta lesão são que a articulação “deslocou” ou “saiu do lugar”.
A entorse consiste em lesões dos ligamentos na região de articulações por traumas torcionais. Popularmente, é conhecida como “torção”. A mais comum é a entorse de tornozelo, embora possa ocorrer em qualquer articulação do nosso corpo.
7. Sobre a articulação do joelho representada no desenho abaixo são feitas algumas afirmações. Julgue-as assinalando a(s) que estiver(em) correta(s).
Articulação do joelho
As articulações do joelho são: Patelo-femoral, Tíbio-femoral, Tíbio-fibular. Em conjunto, realizam movimentos de deslizamento, flexão e extensão.
( V ) Nas extremidades dos ossos em contato temos cartilagens que diminuem o atrito gerado pelo movimento.
( F ) Trata-se de uma articulação ou juntura semimóvel.
( V ) Os ligamentos transmitem a força de contração dos músculos para os ossos
( V ) O líquido sinovial produzido pela articulação também diminui o atrito entre os ossos.
As articulações são classificadas conforme o grau de mobilidade que oferecem. Elas podem ser de três tipos:
Sinartrose, inflexível ou imóvel
São as articulações fibrosas, localizadas entre um osso e outro, caracterizadas por serem inflexíveis. As duas superfícies ósseas são praticamente contínuas, separadas apenas por uma camada de tecido conjuntivo ou cartilaginoso.
Exemplos: a articulação do crânio (sutura), dos dentes e do maxilar, da tíbia e a fíbula.
Anfiartrose ou semi-móveis
São articulações semi-móveis, flexíveis e cartilaginosas. Elas possuem cartilagens entre os ossos e permitem movimentos que evitam o desgaste excessivo dos ossos, auxiliando, dessa maneira, no deslizamento de uns sobre os outros a partir dos diferentes movimentos do corpo.
Exemplos: ossos do quadril e vértebras.
Diartrose ou móveis
São articulações flexíveis, caracterizadas pela presença de bolsas sinoviais, que contém o líquido sinovial ou sinovia, que evita o desgaste ocasionado pelo atrito. Elas localizam-se entre a pele e os ossos.
Exemplos: articulações do ombro, joelhos e cotovelos.
Articulação do manguito rotador no ombro
Articulação do ombro vista em Raio X
As vértebras estão ligadas entre si por 2 tipos de articulações: disco- vertebrais e as interapofisárias. As disco-vertebrais são articulações cartilaginosas formadas pelos corpos e discos intervertebrais, sendo especialmente adaptadas e amortecer e redistribuir o peso.
8. As imagens a seguir apresentam três exames de raios-X de diferentes regiões do corpo humano, onde diversos ossos estão indicados de 1 a 9, e algumas articulações estão indicadas de A a E. Identifique os ossos 1, 4 e 9 e o tipo de articulação em A e C destacados nos raios-X abaixo.
1. Osso 1: Fêmur
A articulação tibiofemoral é uma articulação entre os côndilos lateral e medial da extremidade distal do fêmur e o platô tibial, que são revestidos por uma camada espessa de cartilagem hialina. Articulação móvel.
2. Tibia
3. Fíbula
4. Ileo (Ilium)
5. Cabeça do fêmur
6. Costelas
7. Úmero
8.Costela
9. Clavícula (fraturada)
A. Articulação ou juntura móvel
B. Articulação sinovial do tipo esferóide, que liga o osso da coxa, fêmur, à pelve.
C. Articulações entre vértebras: As vértebras estão ligadas entre si por 2 tipos de articulações: discovertebrais e as interapofisárias. As disco-vertebrais são articulações cartilaginosas formadas pelos corpos e discos intervertebrais, sendo especialmente adaptadas e amortecer e redistribuir o peso. As articulações interapofisárias são sinoviais, ou seja, têm cartilagem hialina, membrana sinovial, osso subcondral e cápsula articular, estando sujeita a artrose como todas as articulações.
D. A articulação glenoumeral é a articulação entre a cabeça do úmero, que tem formato esférico, e a fossa glenoide da escápula.
E. Vértebras cervicais
2. Osso 4: Osso da Pelve ou ilio
Pelve masculina
3. Osso 9: Clavícula
Tipo de Articulação em A: Móvel
As articulação do ombro são Glenoumeral, Acrômio-clavicular e Esternoclavicular. Em conjunto, elas permitem os movimentos de deslizamento, adução e abdução, flexão e extensão, rotação e circundação.
Tipo de articulação em C: Semi-móvel
As vértebras estão ligadas entre si por 2 tipos de articulações: disco- vertebrais e as interapofisárias. As disco-vertebrais são articulações cartilaginosas formadas pelos corpos e discos intervertebrais, sendo especialmente adaptadas e amortecer e redistribuir o peso.
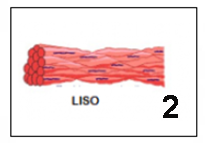
10. Relacione os números das figuras abaixo quanto aos diferentes tipos de músculos com a sua localização.
a) Faça a associação entre os números 1, 2, 3 e 4, e as legendas a seguir:
( 3 ) Extensor contraído;
( 1 ) Extensor relaxado;
( 2 ) Flexor contraído;
( 4 ) Flexor relaxado;
11. Um jogador de vôlei sofreu uma lesão na mão que fez com que tivesse de sair da partida. Analisando a imagem de sua radiografia qual tipo de lesão você acha que pode ter sido? Justifique sua resposta. (2 esc)
Luxação pois deslocou os ossos de sua articulação habitual
Fraturas
12. De acordo com a Organização Mundial de Saúde (OMS), atividade física é qualquer movimento corporal produzido pelos músculos esqueléticos que requeira gasto de energia e seus benefícios são inúmeros. Cite 01 benefício da atividade física sobre o sistema cardiovascular e 01 benefício sobre o sistema locomotor, respectivamente.
A prática de exercícios diminui o risco de infarto agudo do miocárdio, aumenta a sobrevida de pessoas que já tiveram um infarto e pode interferir positivamente em fatores como hipertensão arterial, níveis de colesterol, reabilitação de pacientes pós-infarto, diabetes e obesidade
Com a prática de exercícios como a musculação, por exemplo, ocorre o fortalecimento da musculatura e consequentemente a maior sustentação dos ossos. Com os ossos sendo mais exigidos eles captam mais cálcio e ficam mais fortes evitando assim a osteoporose. Além disso, aumenta a lubrificação das cartilagens, melhora o desempenho das articulações e reduz dores em geral.
Tipos de articulações
As articulações ou junturas podem ser definidas como o local de conexão entre dois ou mais ossos ou destes com as cartilagens. As principais funções desses locais são permitir a movimentação dos segmentos do corpo e manter todos os ossos do esqueleto juntos e estáveis.
De acordo com o tipo de tecido conectivo entre os ossos, as articulações podem ser classificadas em três tipos básicos: fibrosas, cartilaginosas e sinoviais. As articulações fibrosas, também chamadas de sinartroses ou imóveis, possuem uma pequena separação com tecido conjuntivo fibroso e não apresentam cavidade articular (espaço entre as superfícies articulares). A mobilidade dessa articulação é bastante reduzida ou inexistente, porém apresenta certa elasticidade.
Existem dois tipos principais de articulação fibrosa: as suturas e a sindesmoses. O primeiro grupo está relacionado com as articulações do crânio. Já as sindesmoses referem-se à articulação entre tíbia e fíbula e entre o rádio e a ulna.
As articulações cartilaginosas, também chamadas de anfiartroses ou levemente móveis, possuem uma separação cartilaginosa e não apresentam cavidade articular. A mobilidade dessas articulações é reduzida.
Existem dois tipos de articulações cartilaginosas: as sincondroses e as sínfises. Essas últimas possuem entre os ossos cartilagem fibrosa. Como exemplo, podemos citar as articulações presentes entre as vértebras, que possuem entre elas o disco intervertebral. Já as sincondroses possuem entre os ossos cartilagem hialina. A articulação esternocostal, entre o esterno e a cartilagem costal da primeira costela, é um exemplo desse tipo de articulação.
As articulações sinoviais, também chamadas de diartroses ou móveis, possuem uma cavidade articular (cavidade sinovial) que apresenta uma cápsula cheia de líquido sinovial, que funciona como um lubrificante. Essas articulações possuem uma maior liberdade de movimento e são as mais encontradas em nosso corpo.
De acordo com o movimento, as articulações sinoviais podem ser classificadas em uniaxial, biaxial e poliaxial.
Uniaxial – Permite apenas um eixo de rotação. Exemplo: Articulação encontrada entre o úmero e a ulna.
Biaxial – Permite dois eixos de rotação. Exemplo: Articulação do punho.
Poliaxial – Permite três eixos de rotação. Exemplo: Articulação do ombro.
Fontes














































.gif)




